Publié le 30/07/2013 à 22:00
Temps de lecture : 2
min
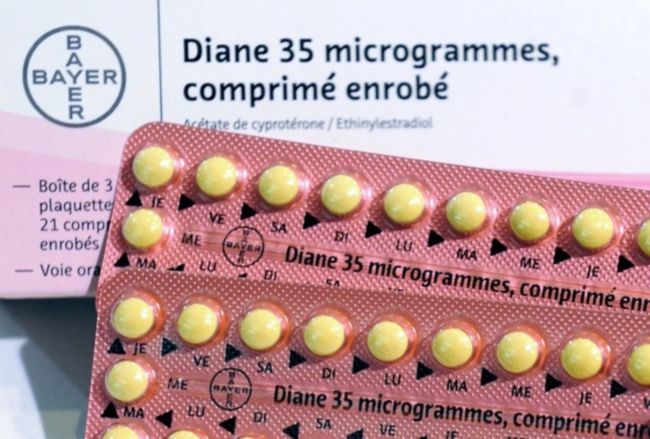
La Commission européenne a imposé mardi à la France de remettre sur le marché le traitement anti-acné Diane 35, largement prescrit comme pilule contraceptive avant son retrait en mai au vu des risques de thrombose.
Prenant en compte les inquiétudes françaises, la Commission a toutefois décidé de restreindre les prescriptions de ce médicament et d'imposer une meilleure information sur ses contre-indications, pour minimiser le risque "connu de thrombo-embolie"
Le laboratoire Bayer devra donc réviser les notices d'utilisations pour y faire figurer ces informations.
Diane 35 sera particulièrement suivi, la Commission a demandé la mise en place d'un plan de gestion des risques dans les trois mois.
Le laboratoire Bayer souligne que, "par cette décision, la Commission européenne a confirmé le profil bénéfice-risque de Diane 35 lorsqu'il est utilisé conformément à son autorisation de mise sur le marché" et que la décision européenne est "applicable à tous les pays de l'UE disposant d'une AMM pour Diane 35", dont la France.
Prenant en compte les inquiétudes françaises, la Commission a toutefois décidé de restreindre les prescriptions de ce médicament et d'imposer une meilleure information sur ses contre-indications, pour minimiser le risque "connu de thrombo-embolie"
Le laboratoire Bayer devra donc réviser les notices d'utilisations pour y faire figurer ces informations.
Diane 35 sera particulièrement suivi, la Commission a demandé la mise en place d'un plan de gestion des risques dans les trois mois.
Le laboratoire Bayer souligne que, "par cette décision, la Commission européenne a confirmé le profil bénéfice-risque de Diane 35 lorsqu'il est utilisé conformément à son autorisation de mise sur le marché" et que la décision européenne est "applicable à tous les pays de l'UE disposant d'une AMM pour Diane 35", dont la France.


